每周抗体药讯20190401-20190407
作者 l 放翁是水货
编辑 l 细胞房间
1
武田制药vedolizumab皮下注射剂型的上市申请在欧盟获得审理
4月1日,日本,武田药业今日宣布欧洲药品管理局已经受理了vedolizumab皮下注射给药用于中度至重度活动性溃疡性结肠炎(UC)或克罗恩病成人治疗的补充申请。此次的补充申请是基于一项关键的III期VISIBLE 1研究,该研究评估了vedolizumab治疗216名中度至重度活动性UC患者的安全性和有效性。试验的数据显示,与接受安慰剂的患者相比,每两周接受维多珠单抗维持治疗的患者其临床缓解率获得显著性差异。此外不良事件发生率(包括严重不良事件和患者感染率)为10.4%,没有导致治疗中止的事件发生。Entyvio®(vedolizumab)是一种特异性拮抗α4β7整合素的生物制剂,此前的静脉注射给药已经获得临床的有效验证。
2
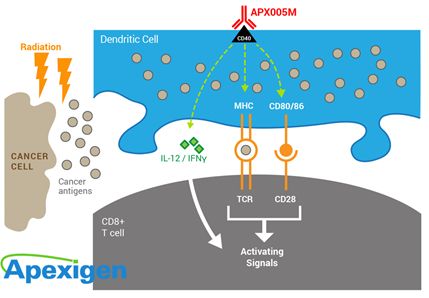
Apexigen公司的胰腺癌新药在初步的临床验证中获得积极进展
4月1日,美国,Apexigen公司今日在AACR大会上展会了APX005M治疗转移性胰腺癌患者的新临床数据,APX005M是一种靶向CD40的单克隆抗体,目前正在不同类型实体肿瘤的多项临床试验中进行评估。正在进行的Ib期临床试验的中期分析显示,24名患有转移性胰腺癌的患者中20名在使用APX005M联合化疗后肿瘤体积缩小,一些患者在治疗一年后仍旧存活并持续接受治疗。
会议第二日,Apexigen公司再次公布了APX005M治疗转移性黑色素瘤的临床数据详情。该Ib期临床数据显示APX005M与nivolumab联合使用时耐受性良好,在抗PD-1治疗无应答且疾病进展的患者中获得了有效的临床应答,试验中未观察到剂量限制性毒性(DLT)。
3
Teva制药的偏头痛药物fremanezumab获得欧盟委员会批准
4月1日,以色列,Teva制药今天宣布,欧盟委员会已授予AJOVY(fremanezumab)预注射注剂型营销许可,用于预防成人患者的偏头痛治疗。AJOVY是人源化单克隆抗体,其与降钙素基因相关肽(CGRP)配体结合并阻断其与受体的结合,是唯一一种用于预防偏头痛的抗CGRP药物。AJOVY已经在两项关键的III期临床试验中进行了评估,试验纳入了患有失能性偏头痛的患者,并研究了fremanezumab作为成人偏头痛预防性治疗的有效性。试验结果显示,与安慰剂相比,接受fremanezumab治疗的患者偏头痛天数明显减少,药物相关不良反应主要是注射部位周围的轻度至中度短暂皮肤反应。
4
Bolt制药公布了其在研新型免疫刺激抗体偶联物的研究进展
4月1日,美国,Bolt Biotherapeutics今天在AACR会议上展示了题为“TLR7/8免疫刺激抗体偶联物引发强健的骨髓激活和持久的抗肿瘤免疫”研究的最新进展。其在研的免疫刺激抗体偶联物(ISAC)在动物模型中显示出良好的根除肿瘤的潜力。与需要瘤内给药的传统TLR激动剂相比,Bolt Biotherapeutics提供的数据证明该新型药物可以全身递送,并在多种癌症模型中表现出抗肿瘤免疫力。在HER2阳性肿瘤模型中,新药物对曲妥珠单抗难治性肿瘤具有同样的抗肿瘤功效,且其具有免疫记忆,对于无HER2抗原表达的同系肿瘤仍具有抗性。
5
K药在中国获批一线治疗非小细胞肺癌适应症
4月1日,中国,默克公司今天宣布KEYTRUDA已获得NMPA批准与培美曲塞和铂类化疗联合使用,用于无EGFR或ALK基因组肿瘤畸变的转移性非鳞状非小细胞肺癌患者的一线治疗。关键的III期KEYNOTE-189试验的数据已经证实患者的总体存活(OS)和无进展存活(PFS)均能获得明显改善。
6
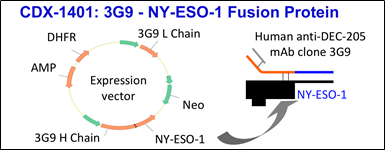
Celldex Therapeutics的抗CD40 抗体疗效获得初步的临床验证
4月2日,美国,Celldex Therapeutics今天在美国癌症研究协会年会上介绍了公司CD40激动剂的最新研究数据。CD40是免疫疗法的重要靶点,在激活先天和适应性免疫反应中发挥关键作用,CDX-1140是一种全人源化抗CD40单克隆抗体,相较于其他抗体具有更强大的生物活性。临床前数据显示激活CD40可通过激活抗肿瘤免疫力和克服对PD-1阻断的抵抗力在癌症免疫治疗中发挥极其重要的作用,现有的临床中期结果表明,CDX-1140是CD40的强效活化剂,与其他关键免疫途径的药物相结合,可以带来显着的临床益处。CDX-1140具有相对于其他CD40激动剂抗体的独特性质:其诱发树突细胞和B细胞活化的有效活性独立于Fc受体相互作用;CD40配体(CD154)结合未被阻断,与天然CD40激活途径有潜在协同作用;并且抗体促进强烈的免疫激活没有重度的不良事件发生。
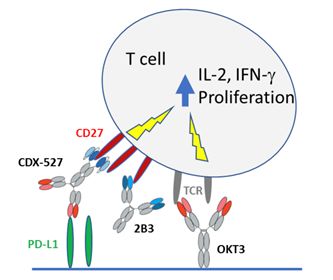
同日,Celldex公司还在会议上展示了该公司候选双特异性抗体药物CDX-527的进展性数据。Celldex公司提供的数据显示,同时具有PD-1阻断和CD27共刺激功能的抗体药物CDX-527比两种单独抗体的组合具有更高的活性。双特异性CDX-527抗体结合了新型的PD-L1抗体用于阻断PD-1检查点途径,结合了CD27激动剂抗体的结合结构域,用于CD27介导的T细胞共刺激。在BCL1淋巴瘤模型中显示出有效的抗肿瘤活性,并且比CD27和PD-L1单克隆抗体的组合显着更有效。非人类灵长类动物的初步研究表明,CDX-527具有良好的药代动力学特性,未观察到毒性。
7
Merus和Incyte公司公布的了双特异性抗体MCLA-145的最新研究数据
4月2日,美国,Merus和Incyte公司在AACR年会上汇报了MCLA-145项目的阶段性研究数据。MCLA-145是一种T细胞激动剂,其在临床前模型中以高亲和力特异性结合人PD-L1和CD137。MCLA-145的独特免疫刺激特性源于其拥有在肿瘤微环境中有效激活免疫效应细胞同时阻断相同免疫细胞群中的抑制信号的能力。此次公布的研究数据显示其拥有多种生物学活性,MCLA-145能以高亲和力结合CD137和PD-L1,其阻断PD-1检查点抑制途径,导致T细胞活化,且与CD137激动剂活性无关。MCLA-145需要在PD-L1阳性细胞存在的情况下特异性诱导CD137信号传导,信号传导强度与PD-L1表达水平直接相关。根据其目前的研究进展,公司预计在2019年第二季度推动MCLA-145进入临床验证阶段。
8
ONS-5010在美国获批开展治疗湿性AMD的III期临床研究
4月2日,美国,Outlook Therapeutics今天宣布FDA已经批准了其候选药物ONS-5010治疗湿性年龄相关性黄斑变性、糖尿病性黄斑水肿和分支视网膜静脉阻塞(BRVO)的临床试验申请,目前该公司将在美国部分地区开始招募患有湿性AMD的患者。ONS-5010是全长人源化抗VEGF(血管内皮生长因子)抗体,能抑制VEGF和相关的血管生成。目前正在开展的关于ONS-5010的III期临床试验旨在湿性AMD患者群中评估ranibizumab与ONS-5010的临床疗效,主要研究重点是患者的平均视力改善情况。
9
Triphase Accelerator启动TRPH-222治疗淋巴瘤的I期临床研究
4月2日,加拿大,Triphase生物医药公司今天宣布其在研候选药物TRPH-222治疗淋巴瘤患者的I期临床研究已经有第一名受试者入组接受给药。这项临床试验是TRPH-222单药治疗复发和/或难治性B细胞非霍奇金淋巴瘤(NHL)的多中心,开放性研究,目前正在美国和加拿大的研究所招募患者。TRPH-222是一种靶向CD22新型位点的特异性抗体药物偶联物,CD22是B细胞限制性唾液酸糖蛋白,是B细胞信号传导和存活的重要调节剂,几乎在所有恶性肿瘤B细胞上表达。其作为非霍奇金淋巴瘤(NHL)和急性淋巴细胞白血病(ALL)的靶点效应也已经过临床验证。

10
原发性体液免疫缺陷病(PIDD)抗体新药在美国获批
4月2日,美国,ADMA生物制品公司今日宣布FDA已批准ASCENIV™(静脉注射免疫球蛋白药物)用于治疗成人和青少年的原发性体液免疫缺陷病(PIDD)。原发性免疫缺陷病是一组少见病,与遗传相关,常发生在婴幼儿,患者表现为反复感染,严重者会威胁生命。按免疫缺陷性质的不同,可分为体液免疫缺陷为主、细胞免疫缺陷为主以及两者兼有的联合性免疫缺陷三大类。此外,补体缺陷、吞噬细胞缺陷等非特异性免疫缺陷也属于此组疾病。
11
以EphA3为靶点的单克隆抗体ifabotuzumab获得初步的临床验证
4月2日,美国,Humanigen公司今日公布了抗EphA3单克隆抗体ifabotuzumab在复发性GBM患者中的I期临床研究进展。该研究表明,使用ifabotuzumab治疗可快速且特异性靶向肿瘤微环境,对肿瘤血管生成具有直接影响作用,暗示靶向EphA3抑制肿瘤新血管生成是治疗实体肿瘤的一个可行策略。
12
Pieris制药展示了双特异性抗体PRS-342的临床前研究数据
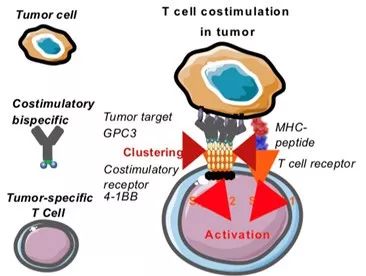
4月3日,美国,Pieris Pharmaceuticals今天公布了其新研发的双特异性抗体候选药物PRS-342的最新研究数据。这篇题为“GPC3/4-1BB双特异性分子共刺激剂PRS-342能够的刺激T细胞,导致人源化HCC小鼠模型中T细胞活化和肿瘤生长抑制”的海报,清晰展示了该候选药物能够导致NF-κB活化,刺激T细胞激活,IL-2的表达量增加并具有剂量依赖性关系。PRS-342还能诱导人源化肝细胞癌异种移植小鼠模型中肿瘤浸润淋巴细胞(TIL)水平局部增加,所呈现的数据表明PRS-342具有潜在抗肿瘤活性。
13
Rgenix公司公布了抗MERTK抗体药物的最新研究数据
4月3日,美国,Rgenix公司今天公布了正在进行的RGX-019研究的临床前数据。RGX-019是一种单克隆抗体,其选择性靶向MERTK(TYRO3/AXL/MERTK家族受体酪氨酸激酶),MERTK在免疫细胞如巨噬细胞,树突细胞和NK细胞中表达,并且在多种液体和实体癌中也过表达。Rgenix公司的数据显示RGX-019以高亲和力和选择性结合人MERTK,而不与其他相关TAM激酶可检测结合。RGX-019具有独特的作用机制,不仅阻断配体结合,还可以通过受体内化导致MERTK降解。这种新的作用机制所展现的作用是在体外和体内抑制癌细胞的生长,促进免疫抑制性M2巨噬细胞释放M1(促炎)细胞因子。
14
CytomX制药的新药CX-2009获得初步的临床疗效验证
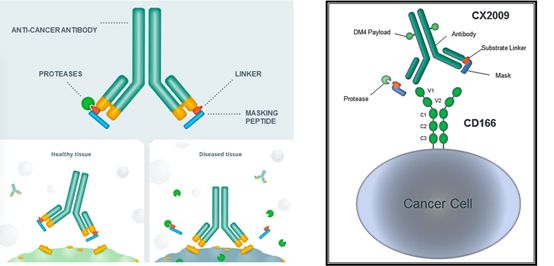
4月3日,美国,CytomX制药今天在AARC会议上公布了其在研新药CX-2009(靶向CD166的前体药物偶联物,PDC)的研究数据。这是一种新型的靶向CD166抗癌药物,该药的首次人体研究评估在七种选定肿瘤患者中CX-2009的安全性和抗肿瘤活性。在71名可评估疗效的患者中,74%的患者在第一次治疗后疾病稳定或好转,38%的患者其肿瘤体积缩小。最常见的治疗相关不良事件包括恶心、疲劳和食欲下降。
小编点评:鉴于CD166在正常组织中的广泛表达,CX-2009的安全性需要特别值得注意。
15
Agenus公司的新一代抗CTLA-4抗体药物进入I期临床研究
4月3日,美国,Agenus公司其抗CTLA-4抗体(AGEN1181)的临床研究已经获得第一位受试者入组。这项开放标签,多中心研究旨在评估AGEN1181在晚期实体瘤患者中的最大耐受剂量,同时还将评估该抗体的安全性、耐受性、PK和PD参数以及免疫原性。AGEN1181是一种具有增强抗肿瘤功能潜力的新型Fc工程化抗体,专门用于协同现有抗肿瘤疗法,增强其抗肿瘤活性。
16
Jounce公司公布了巨噬细胞免疫检查点抑制剂JTX-8064的研究数据
4月3日,美国,Jounce Therapeutics今天在AACR年会上展示了其首个抗白细胞免疫球蛋白样受体B2(LILRB2)抗体的研究数据。现有的临床前数据显示JTX-8064是LILRB2的特异性强效拮抗剂抗体,LILRB2与其配体结合并在巨噬细胞中维持免疫抑制状态,JTX-8064阻断配体与LILRB2的结合并诱导巨噬细胞中的免疫激活状态,可能导致抗肿瘤免疫反应增强。所有证据支持JTX-8064具有在肿瘤微环境中可以重新编程肿瘤相关巨噬细胞以增强抗肿瘤免疫力的潜力,其可作为巨噬细胞的免疫检查点。
17
Aptevo Therapeutics公司公布了两个双特异性抗体的新研究数据
4月3日,美国,Aptevo Therapeutics公司今天公布了两种双特异性抗体APVO436(一种靶向CD123和CD3的双特异性抗体)和APV-527(一种靶向4-1BB和5T4的双特异性抗体)的临床前研究数据。APVO436在体内具有良好的耐受性,在CD123阳性肿瘤靶细胞存在下能诱导CD4和CD8 T细胞的激活和增殖,与同类型的分子相比,具有更可控的细胞因子释放特征。APVO436目前正在AML和MDS患者的I期临床试验中进行评估。APV-527临床前数据显示在存在5T4抗原阳性的肿瘤环境中能够选择性的免疫激活,且在剂量范围毒理学研究中耐受良好。5T4抗原存在于许多不同类型的实体瘤上,包括非小细胞肺癌,头部和颈部癌症,间皮瘤和胰腺癌等。
18
IDACIO(阿达木单抗生物仿制药)在欧洲获批上市
4月5日,德国,Fresenius Kabi公司最近宣布欧盟委员会已经批准IDACIO(阿达木单抗生物仿制药)的上市许可,并拥有参比制剂的所有适应症。IDACIO是Fresenius Kabi公司生物仿制药产品组合中第一个获得批准的产品,其在健康志愿者和患者中的临床数据均有参比制剂一致,可用于未来临床中的替换用药。相信能够给类风湿性关节炎、青少年特发性关节炎、轴性脊柱关节炎、银屑病关节炎、斑块状银屑病、克罗恩病、溃疡性结肠炎等患者带来更经济的治疗选择。
19
Celgene公司和Acceleron公司递交了luspatercept的上市申请
4月5日,美国,Celgene公司和Acceleron公司今天宣布已经递交了luspatercept的上市申请,寻求将该药用于红细胞成熟剂骨髓增生异常综合征(MDS)相关性贫血和β地中海贫血相关性贫血的治疗。MDS或β地中海贫血患者目前在临床上有很高的医疗需求,现有的支持疗法是慢性输注红细胞,但这种疗法有可能引起患者体内的铁超负荷和其他并发症。Luspatercept这种研究性疗法还需要在真实世界进行更大样本的临床验证,目前该药未在任何国家获批上市。
欢迎加入小编团队成为小编一员
请加小编微信号:wuwenjun7237
如有技术解读、行业洞见愿意分享
欢迎投稿到小编邮箱:wuwj06@163.com

欢迎个人转发分享。其他任何媒体、网站如需转载或引用本网版权所有内容须获得授权且在醒目位置处注明“转自:生物制药小编”。

坚持原创、坚持专业
欢迎关注生物制药小编
投稿信箱:wuwj06@163.com
小编团队现有21位成员:
Armstrong、医药局外人、Fairy、Jone、东胜西牛、Alpharesearcher、MT、百草、Irene、Self Renew、蛋白工人、At.Zhou、Julia、游方和尚、Grand、夕阳武士、吃瓜群众、Nathan、神经元、Clear兮、南山南
欢迎有共同兴趣的朋友加入

扫码实时看更多精彩文章



