每周抗体药讯20190101-20190106
作者 l 放翁是水货
编辑 l 细胞房间
1
信达生物关于晚期食管癌的III期临床研究正式开始
1月1日,中国,信达生物今天宣布评估Tyvyt®(全人源化抗PD-1治疗性单克隆抗体,sintilimab注射液)与紫杉醇和顺铂联合用作晚期复发或转移性食管鳞状细胞癌(ESCC)一线治疗的III期临床试验(ORIENT-15)已经在多个中心顺利开展,目前已经有第一位受试者入组治疗。ORIENT-15研究是一项随机,双盲,多中心临床试验,该研究计划招募640名合适患者,旨在评估Tyvyt®或安慰剂联合化疗作为一线治疗食管癌的疗效和安全性,主要终点是患者的总体存活率。
小编点评:食管癌是我国第三大常见恶性肿瘤,亚洲国家食管鳞状细胞癌的发病率远高于西方国家,目前化疗和放射治疗外,患者没有其他治疗选择,新的临床数据显示,免疫检查点抑制剂为这种类型的肿瘤患者带来了新的希望。
2
Harpoon公司治疗前列前癌的新药I期临床取得阶段性进展
1月2日,美国,Harpoon Therapeutics今天宣布评估其治疗转移性去势抵抗性前列腺癌(mCRPC)的创新药HPN424的I期临床研究已经获得初步进展。这项开放标签,剂量递增和剂量拓展研究旨在评估HPN424的安全性、耐受性、药代动力学和临床活性。已有的针对7名患者的试验数据显示,其中3名患者循环系统中的肿瘤生物标记物明显减少,外周细胞因子和趋化因子水平上升并呈现计量递增关系,暗示患者体内的T细胞被激活。迄今为止未观察到与剂量相关的毒性时间,患者常见的不良反应包括发热、细胞因子释放综合征等。截止目前,两名患者疾病相对稳定,其余患者的疾病负担均在承受范围内并持续进行治疗。
HPN424是一种新型T细胞生物制剂,能够特异性靶向前列腺特异性膜抗原,属于T细胞激活构建体,通过以靶标依赖性方式激活T细胞。

3
Sesen Bio公布了Vicinium治疗非肌层浸润性膀胱癌的III期临床初步数据
1月3日,美国,Sesen Bio公司今日宣布其正在进行的III期临床VISTA试验在临床疗效方面已经取得积极的结果。VISTA试验是一项开放标签、多中心III期临床试验,旨在评估Vicinium®对晚期非肌层浸润性膀胱癌(NMIBC)患者的疗效和耐受性。该试验的主要终点是患者的乳腺疾病或非乳头状疾病的完全缓解率,试验中的患者每周两次接受Vicinium的局部给药治疗,持续六周,然后每周一次给药再持续治疗六周,最后依据患者病情进展每隔一周接受治疗,最多维持治疗两年。报告的数据显示,在完成第一步治疗后,试验分别随访了3个月、6个月、9个月和12个月,并评估了原位癌患者的完全缓解率。虽然尚未达到中位数,但初步统计显示Vicinium治疗导致多数患者的持续应答时间延长,通过延迟根治性膀胱切除术的时间患者获得更多受益。在VISTA试验中接受治疗的患者对Vicinium的耐受性良好,截至2018年12月3日的数据截止,在所有三个队列(n = 133)的患者中,78%的不良事件为1级或2级。最常报告的治疗相关不良事件为排尿困难(13%),血尿(12%)和尿路感染(11%)。
Vicinium®是一种局部给药的融合蛋白,该候选产品主要用于治疗晚期非肌层浸润性膀胱癌。 该产品由重组融合蛋白组成,可以特异性靶向肿瘤细胞表面上的上皮细胞粘附分子(EpCAM),其通过基因工程肽链携带的假单胞菌外毒素A可以定向摧毁肿瘤细胞。此外,Sesen Bio前期的临床数据显示Vicinium的癌细胞杀伤特性同样能促进了抗肿瘤免疫反应,与肿瘤免疫药物的联合使用具有良好的协同抗肿瘤作用。

4
Viela Bio公司关于视神经脊髓炎谱系障碍疾病的关键III期临床取得突破性进展
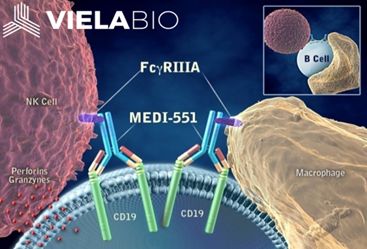
1月3日,美国,Viela Bio今天宣布一项关于inebilizumab治疗视神经脊髓炎谱系障碍(NMOSD)的关键试验达到了主要和关键的次要终点。这是一项随机、双盲、安慰剂对照的全球多中心临床研究,共招募了231名患有NMOSD的患者,以评估inebilizumab对于降低NMOSD发作风险的有效性。初步分析显示,与安慰剂相比,接受inebilizumab单药治疗的患者NMOSD发作风险降低了77%,此外受试患者的残疾恶化也相应减少。
NMOSD是一种罕见的中枢神经系统自身免疫性疾病,约80%的患者能自发产生水通道蛋白-4(AQP4)自身抗体。已知高表达CD19的B细胞包括浆母细胞和浆细胞在NMOSD的发病机制中发挥关键作用,这些AQP4-IgG自身抗体由浆母细胞和浆细胞产生,并主要与中枢神经系统中的星形胶质细胞结合。异常的免疫反应会导致体内正常的视神经和脊髓细胞受到攻击,这一连锁的损伤效应常导致患者发生严重的肌肉无力甚至瘫痪,视力丧失、呼吸衰竭、肠和膀胱功能问题也是该疾病的常见并发症。Inebilizumab是一种人源化单克隆抗体,以高亲和力结合分泌抗体的浆母细胞和浆细胞表面的CD19,在与CD19结合后,这些细胞迅速从循环系统中耗尽。
小编点评:这项研究证明了CD19阳性B细胞是此类疾病的重要驱动因素,同时也证明了inebilizumab能够有效降低NMOSD发作风险,为患者提供了一种新的用药选择,对于未来临床的诊疗具有重要意义。
5
Biogen公司开发多发性硬化症改良疗法的III期临床正式开始
1月3日,美国,Biogen今日宣布开展一项新的NOVA研究,以评估延长natalizumab给药间隔的新疗法与标准疗法相比在复发性多发性硬化症治疗方面的疗效和安全性,目前该项全球IIIb期研究已经有第一位患者受试治疗。新NOVA研究是一项为期两年,前瞻性、随机、对照的开放标签试验,重在评估那他珠单抗六周一次的给药方式对于多发性硬化症的疗效。该研究将招募全球约480名患者,研究的主要终点是48周时患者新增的T2高信号病变的数量。
TYSABRI®(那他珠单抗)已在80多个国家获得批准,在美国TYSABRI主要用于治疗复发型MS患者。TYSABRI增加了机会性病毒感染的风险, TYSABRI还增加了由单纯疱疹和水痘带状疱疹病毒引起的脑炎和脑膜炎的风险。在TYSABRI治疗的患者中发生的其他严重不良事件主要是过敏反应和感染,临床上也有显着肝损伤的案例报道,因此改良现有疗法是降低不良事件发生率,提高用药安全的重要工作。
6
AbbVie携手Tizona共同推进CD39靶向药物的临床开发
1月3日,美国,AbbVie公司今天宣布已经与Tizona Therapeutics达成全球战略合作,共同开发和商业化CD39靶向药物TTX-030,推进其在癌症领域的临床研究。已有的研究显示ATP-adenosineaxis通过控制免疫细胞的炎症和抑制活性而成为肿瘤微环境(TME)中的免疫调节开关。在TME中,CD39是负责将细胞外ATP转化为免疫抑制性腺苷的酶,用TTX-030抑制CD39,可能是一种新型的激活免疫应答的新途径。根据协议条款,Tizona已获得1.05亿美元的预付款,用于靶向CD39药物的独家开发费用,此外AbbVie已对Tizona进行股权投资。Tizona保留了在美国共同开发和共同推广的选择权,并有资格获得成功的开发和商业里程碑以及净销售额的相关分成。
TTX-030是一种单克隆抗体,可抑制CD39的活性,CD39催化ATP转化为AMP,这是腺苷生成的重要步骤。通过阻断CD39的作用,TTX-030阻止免疫抑制性细胞外腺苷的形成,以有效维持肿瘤微环境中效应细胞的活性。除此以外,TTX-030还能阻止ATP的降解,保留其刺激树突状和髓样细胞的能力。
欢迎加入小编团队成为小编一员
请加小编微信号:wuwenjun7237
如有技术解读、行业洞见愿意分享
欢迎投稿到小编邮箱:wuwj06@163.com

欢迎个人转发分享。其他任何媒体、网站如需转载或引用本网版权所有内容须获得授权且在醒目位置处注明“转自:生物制药小编”。

坚持原创、坚持专业
欢迎关注生物制药小编
投稿信箱:wuwj06@163.com
小编团队现有21位成员:
Armstrong、医药局外人、Fairy、Jone、东胜西牛、Alpharesearcher、MT、百草、Irene、Self Renew、蛋白工人、At.Zhou、Julia、游方和尚、Grand、夕阳武士、吃瓜群众、Nathan、神经元、Clear兮、南山南
欢迎有共同兴趣的朋友加入

扫码实时看更多精彩文章



